医疗器械注册咨询
所属分类: 生产许可证
医疗器械注册是食品药品监督管理部门根据医疗器械注册申请人的申请,依照法定程序,对其拟上市医疗器械的安全性、有效性研究及其结果进行系统评价,以决定是否同意其申请的过程。
我们的服务对象
(1) 国内外医疗器械生产企业
(2) 医疗器械研发单位
(3) 医疗器械流通单位
(4)有销售网络和经验的从事医疗器械代理的自然人
(5)其它
医疗器械注册是食品药品监督管理部门根据医疗器械注册申请人的申请,依照法定程序,对其拟上市医疗器械的安全性、有效性研究及其结果进行系统评价,以决定是否同意其申请的过程。
我们的服务对象
(1)国内外医疗器械生产企业
(2)医疗器械研发单位
(3)医疗器械流通单位
(4)有销售网络和经验的从事医疗器械代理的自然人
(5)其它
注册分类
(1)国产医疗器械首次注册
(2)国产医疗器械重新注册
(3)进口医疗器械初次注册
(4)进口医疗器械延续注册
在我国,第二类、第三类医疗器械实行注册管理。
境内第一类医疗器械备案,备案人向设区的市级食品药品监督管理部门提交备案资料。
境内第二类医疗器械由省、自治区、直辖市食品药品监督管理部门审查,批准后发给医疗器械注册证。
境内第三类医疗器械由国家食品药品监督管理总局审查,批准后发给医疗器械注册证。
进口第一类医疗器械备案,备案人向国家食品药品监督管理总局提交备案资料。
进口第二类、第三类医疗器械由国家食品药品监督管理总局审查,批准后发给医疗器械注册证。
第一类医疗器械产品备案和申请第二类、第三类医疗器械产品注册,应当提交下列资料:
(一)产品风险分析资料;
(二)产品技术要求;
(三)产品检验报告;
(四)临床评价资料;
(五)产品说明书以及标签样稿;
(六)与产品研制、生产有关的质量管理体系文件;
(七)证明产品安全、有效所需的其他资料。
工作程序
与企业初步接触,了解企业有关注册的意图;
研究企业欲注册产品的相关资料,并向企业提出反馈意见;
与企业确立合作关系,我公司成立项目小组;
向企业提供制作申请资料所必须的文件清单;
编制注册产品标准;
医疗器械注册检测(如需要);
指导企业完成质量体系考核(如需要);
指导企业完成临床试验(如需要);
在规定的时间内完成申报资料的制作;
向国药局提交注册申报资料;
根据行政部门的审评意见,指导客户完成审批过程中资料的修改与补充;
获得注册证。
益处
医疗器械注册证书样本,仅供参考。
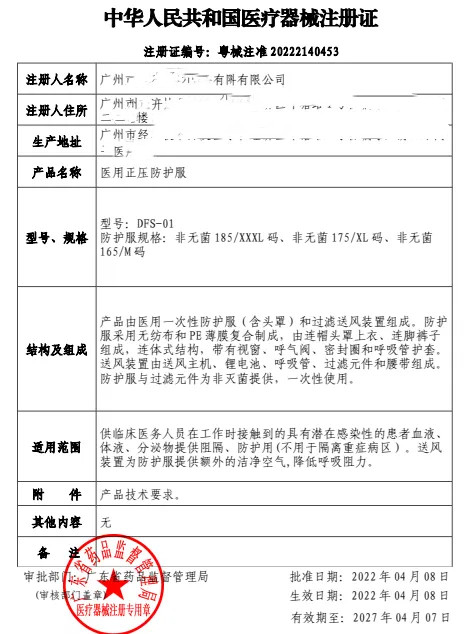
作为专业化的医疗器械咨询公司,我们是医疗器械企业可借用的有效外部资源。公司在长期稳定地发展中积聚了一批高级人才和业内精英,同时还形成了专家教授学术层、学会、协会现行法规及实质操作支持层。并与国内外知名的医学院校、科研院所、实验室和临床医院建立了稳固的合作关系,实现人力、技术、信息、资源的综合优势。
公司在为政府、学会、协会长期的服务过程中,与其建立了良好的协作关系,因此我公司能随时了解和掌握国家药品食品监督管理局在医疗器械注册方面的前沿信息和最新政策。
公司从事医疗器械注册的队伍是由具有丰富注册经验、熟悉医疗器械注册法规和技术要求的专业人员组成。
公司和多所大专院校及研究所有合作关系,可充分的利用相关科技优势为客户服务。
更多资讯,请点击:http://www.twgrace.com/或拔打:020-38849876/13066329278


